안녕하세요. 결국 HLB가 미국의 식품의약국으로부터 리보레사립과 캄렐리주맙의 병용요법이 간암 치료제 불허를 받았다고 하였는데요.
CRL(보완요구서완)을 통보 받았다고 하였습니다. 이에 대해서 HLB 회장인 진양곤 회장은 FDA에서 보내온 문서는 리보세라닙의 문제가 아닌 중국 항서제약의 캄렐리주맙의 문제라고 하였는데요.
항서제약이 FDA 화학제조품질관리(CMC) 실사과정에서 지적을 받았음에도 이에 대한 변론을 준비하지 않은 것이 문제가 되었다고 하였습니다. 리보세라닙은 HLB가 글로벌 특허권을 가지고 있는 표적항암제로 리보세라닙과 캄렐리주맙 병용요법은 표적함암제와 면역항암제를 함께 사용한 첫번째 사례로 큰 기대를 받은 상황이라고 하였는데요.
모든 환자군의 치료가 가능하고 부작용이 적기 때문에 큰 기대를 받는 중이었다고 하였습니다. 하지만 결국 항서제약의 실수로 물거품이 되었다고 하였는데요.
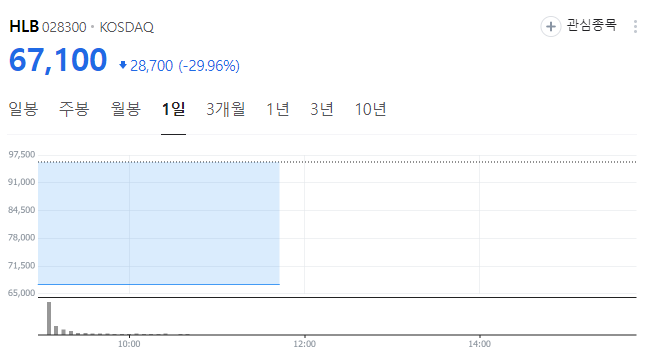
이에 현재 주가는 67,100원으로 하한가를 기록하는 중이라고 하였습니다. 기대가 큰 만큼 하락...
#HLB이노베이션
#HLB
#HLB글로벌
#HLB생명과학
#HLB제약
#HLB테라퓨틱스
#하한가
#보완요구서한
#HLB파나진
#CRL
#HLB바이오스테
#FDA
#항서제약
원문링크 : HLB 美 FDA 승인 불발, 하한가 대처 방안은?

![[카밀라해리슨관련주] 미국의 대통령 후보 카밀라 해리슨, 새로운 경제정책 공개](https://mblogthumb-phinf.pstatic.net/MjAyNDA4MTlfMTA1/MDAxNzI0MDA4MDkyMDk4.gXU7yPV0qb8djEFPsMh8W3DyslzPcia0ScQenwVbU7wg.uCKHIH_bVpcHySLfcQfrVp7NqaHaK7w7qn78ZWrJU-Ug.PNG/image.png?type=w2)