1. 물의 전기 분해란?
2. 물의 전기 분해 화학반응식 분석 3.
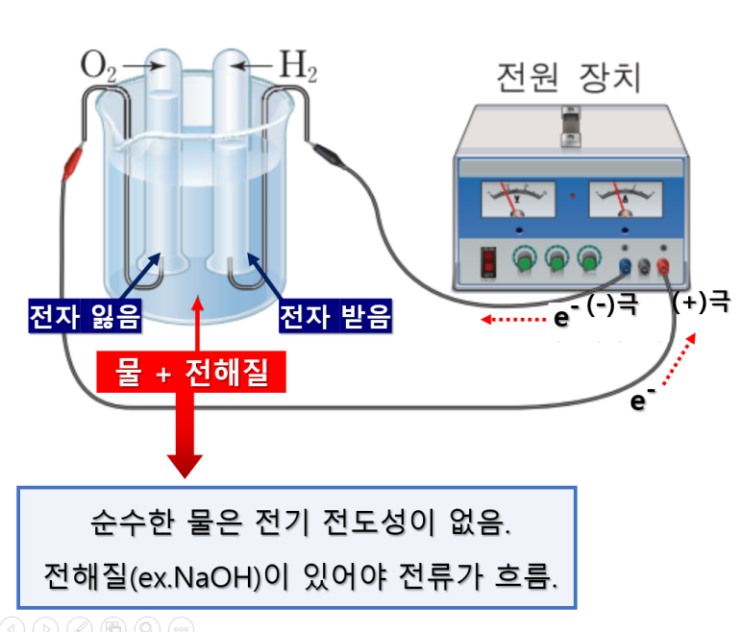
전해질 원리 및 분석 물의 전기 분해란? 물의 전기 분해 장치는 다음과 같이 생겼습니다.
전원 장치에서 전류를 내보내고, 전극은 물과 연결되어 있습니다. 전자(e-)는 (-)극에서 (+)극으로 이동합니다.
각각의 전극은 유리관으로 덮어 발생하는 기체를 모으는 것이지요. 여기서 잠깐 H2O의 특징을 보자면, 물 분자(H2O) 중 매우 극소수는 H2O → H+ + OH- 스스로 "이온화"가 되는 특성이 있습니다.
(물의 자동 이온화) 이온화된, H+ 와 OH-가 각각의 전극에서 수소 기체와 산소 기체가 되는 것이지요. 또한, 물은 매우 극소수만 스스로 이온화되므로, 순수한 물은 전기전도성이 없습니다.
따라서 전류가 흐를 수 있도록 추가로 "전해질"을 넣어주어야 합니다. 각각의 (+), (-) 전극은 (-)극 : H가 전자를 받음.
H2기체 생성↑ (+)극 : O가 전자를 잃음. O2기체 생성↑ 화학 반응식 2H2O → ...
#산화
#양극
#음극
#음이온
#전기분해
#전기화학
#전자
#전해질
원문링크 : 물의 전기분해 원리를 알아보자